电化学电池指的是化学能与电能互相转化的装置,它可以分为原电池和电解池两大类。原电池能自发地将化学能转化为电能;电解池则需要消耗外部电源提供电能,使电池内部发生化学反应。很多电池当实验条件改变时,原电池和电解池能相互转化。
电化学电池是化学能与电能互相转化的一种电化学反应器。如果自发地将化学能变成电能,这种电化学电池称为原电池;如果实现电化学反应的能量由外电源供给,则这种电化学电池称为电解池。原电池将化学能转变为电能,电解池将电能转变成化学能。每个电化学电池都由两个称之为电极的导体和与之接触的电解质溶液构成。一支电极和与其相接触的电解质溶液构成一个半电池,两个半电池构成一个电化学电池。
在电化学电池中,发生氧化反应的电极称为阳极,发生还原反应的电极称为阴极。在右图所示的铜-锌原电池中,阳极和阴极上发生的氧化还原反应如下:
阳极(锌极、负极):Zn-2e→Zn2+
阴极(铜极、正极):Cu2++2e→Cu
锌电极发生氧化反应,锌棒上的Zn原子由固相进入液相成为Zn2+;铜电极发生还原反应,溶液中的Cu2+由液相进入固相成为Cu原子。电子的传递和转移通过连接两电极的外电路导线完成。因为电子由锌极流向铜极,故铜极为正极,锌极为负极(电极的“阴”、“阳”是根据电极反应性质确定的;电极的“正”、“负”是根据电极电位高低确定的)。在电池内部,两电解质溶液通过KCL盐桥相接触。当电极发生氧化还原反应时,ZnSO4烧杯中溶液富正电荷,CuSO4烧杯中溶液富负电荷,这时盐桥中的Cl-向ZnSO4溶液中迁移,K+向CuSO4溶液中迁移,由此构成电流回路。
原电池的总反应为:Cu2++Zn→Cu+Zn2+
按照习惯,把阳极及与其相接触的溶液写在左边,把与阴极相关的部分写在右边;半电池中的相界面以单竖线“|”表示;两个半电池通过盐桥连接时以双竖线“║”表示;溶液注明活(浓)度,气体注明压力,若不特别说明,温度系指25℃。铜-锌原电池的符号可表示为:
(一)Zn|ZnSO4(1mol/L)║CuSO4(1mol/L)|Cu(+)
若外加电压大于原电池的电动势,则铜-锌原电池变成电解池:
阳极(铜极、正极):Cu-2e→Cu2+
阴极(锌极、负极):Zn2++Cu→Zn
电解池的总反应为:Zn2++Cu→Zn+Cu2+
上述反应是铜锌原电池反应的逆反应。显然,原电池的电池反应自发进行;电解池的电池反应不能自发进行。在电位法中使用的测量电池均为原电池。
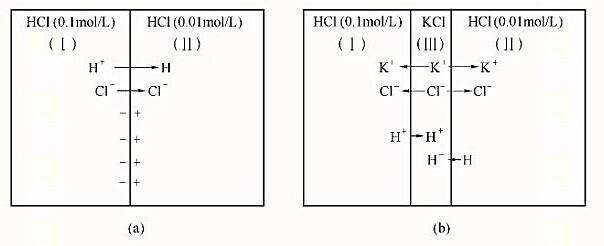
当组成不同或浓度不同的两种电解质溶液接触形成界面时,在界面两侧产生的电位差称为液体接界电位,简称液接电位,记为Ej。离子在溶液中扩散速率不同是产生液接电位的主要原因。根据实际测量,0.1mol/LHCL(Ⅰ)与0.01mol/LHCL(Ⅱ)接触时(如右图a)Ej大约为40mV。由于Ej很难准确测量,而进行电位法测量的电化学电池多为有液接的电池,因此必须设法消除或减小Ej的影响。一般通用的做法是在两个电极溶液之间设置盐桥,内充高浓度KCL(或其他合适的电解质)溶液。由于K+和Cl-的扩散速率很接近,所以当盐桥与不太浓的电解质溶液接触时,占压倒优势的扩散将是Ⅲ相中K+和Cl-几乎同时进入Ⅰ相和Ⅱ相(如右图b),由此使Ej变得很小(1~2mV),一般可以忽略不计。
在电位法中,盐桥具有以下作用:将正负两极电解质溶液分开,避免其互相混合;沟通内电路;消除或减小液体接界电位;保护参比电极内充液不受试液沾污,以使电极电位恒定。作为盐桥的一般条件是:
①盐桥中正负离子扩散速度大致相等;
②浓溶液与电解质溶液接触时,以盐桥中正负离子扩散为主;
③不与组成电池的溶液发生反应,如溶液中有Ag+,则不可用KCL作盐桥(可选用KNO3)。